Esta
aula ocorreu com alunos do 1º ano. Foi explicado configuração
eletrônica e depois fez-se um jogo: Origami na distribuição
eletrônica. Nesse jogo foram feitos origamis em forma de cubo e em
cada cubo constava o nível e o subnível, um número atômico era
dado e o elemento a qual pertencia a partir disso o aluno fazia sua
configuração, depois pegavam os origamis correspondentes aos níveis
e subníveis desejados e acrescentavam a quantidade de elétrons
certas em cada subnível até completar o número atômico pedido.
Depois foi feita toda a configuração com os origamis e colocada na
cartolina e ficou exposta na sala.
Este blog foi criado sob o propósito de divulgar as atividades realizadas pelo subprojeto de Química do PIBID 2011 da Universidade Estadual Vale do Acaraú nas escolas parceiras e no espaço acadêmico dos bolsistas. Além disso, focado na divulgação da ciência, esse blog propõe-se a abordar a Química de um jeito mais real, fornecendo várias abordagens de temas afins a Química e que mereciam ser revistos pelo docente formado e em formação. Aproveitem!
Total de visualizações de página
terça-feira, 27 de novembro de 2012
segunda-feira, 27 de agosto de 2012
10º Simpósio Brasileiro de Educação em Química
A comissão organizadora do SIMPEQUI
realiza anualmente um encontro a fim de reunir todos os profissionais
relacionados à área de química, em particular, aqueles que trabalham na
educação e no ensino de química.
O 10º encontro anual teve como
temáticas à educação em química e mais especificamente a diversidade no ensino
em química, o encontro realizou-se nos dias 29 a 31 de julho em Teresina no
estado do Piauí.
A programação do SIMPEQUI teve
inicio domingo as 16:30 com a abertura da Secretaria Retirada de Materiais em
seguida com a Abertura Oficial e logo após a Palestra de Abertura. O evento
contou ainda com apresentação de pôsteres a palestras nos dias 30 e 31 de
julho.
O evento contou com a participação
de Airton Marques da Silva, Álvaro Chrispino, Ana Cristina Facundo de Brito,
Áttico Chassot, Clara Virgínia Vieira Carvalho Oliveira Marques, Cleide Maria
da Silva Leite, Davi da Silva, Èdson Cavalcante da Silva Filho, Florinda do
Nascimento Cersosimo, Francilio de Carvalho Oliveira, Geraldo Eduardo da Luz Junior,
Os bolsistas do subprojeto de Química do PIBID UVA 2011 juntamente com seu coordenador de área, participaram desse encontro de tema tão relevante para um curso de licenciatura em química contribuindo para a formação dos referidos alunos como também para a divulgação das ideias inovadoras que estão sendo postas em prática na Universidade Estadual Vale do Acaraú.
Química no Intervalo
Com o intuito de apresentar aos alunos das escolas participantes do
PIBID-QUIMICA sobre a perspectiva de atuação da atividade científica ou lúdica,
como forma de acrescentar um intervalo de melhor qualidade na escola, motivando cada aluno a ser futuro pesquisador,
utilizando materiais da própria região.
Os alunos do PIBID-UVA e alunos da Iniciação
Científica dos laboratórios de pesquisa de química da UVA apresentaram seus
trabalhos, em forma de Banner, aos alunos da escola.
35ª Reunião Anual da Sociedade Brasileira de Química - RASBQ
Na 35ª Reunião Anual da Sociedade Brasileira de Química-RASBQ 3 trabalhos do subprojeto de Química do PIBID UVA 2011 foram aprovados e apresentados em forma de poster, divulgando os trabalhos da Universidade e promovendo a interação entre alunos de diversas regiões do país.
quarta-feira, 25 de abril de 2012
Como Funciona o Filtro solar?
O que é?
O filtro solar (também conhecido como protetor solar) é uma loção, spray ou produto tópico que ajuda a proteger a pele da radiação ultravioleta do sol, o que reduz as queimaduras solares e outros danos à pele, ultimamente ligado a um menor risco de câncer de pele. Entretanto, a loção de bronzeamento é um termo incorreto para o filtro solar, já que sua função é completamente diferente.
A loção de bronzeamento é usada para atrair raios UV para atingir um melhor bronzeado.Estas são comumente projetadas para o uso em piscinas se projetada ao ar livre pode ou não ter protecção FPS.
Os melhores filtros solares protegem tanto para UVB (radiação ultravioleta com comprimento de onda entre 290 e 320 nanometros), que pode causar queimaduras solares, e UVA (entre 320 e 400 nanometros), que causa efeitos danosos à pele a longo prazo, como envelhecimento prematuro da pele.
Muitos protetores solares contem tanto compostos orgânicos química orgânica que absorve a luz ultravioleta (como o oxibenzeno) ou um material opaco que reflete a luz (como o dióxido de titânio, o óxido de zinco), ou uma combinação de ambos. Tipicamente, materiais absortivos são referidos como bloqueadores químicos, já os materiais opacos como bloqueadores minerais ou físicos.
A dosagem para o filtro solar pode ser calculada usando a fórmula para a área de superfície do corpo e subsequentemente subtraindo a área comberta por roupa que dá proteção efetiva contra a radiação UV. A dose usada pela FDA nos testes de filtro solar é de 2 mg/cm². De uma amostragem calculada em uma monografia da FDA, se assumirmos um adulto mediano com altura de 1,63 m e peso de 68 kg com 82 cm de cintura, ele necessitaria de exatamente 29 g para cobrir sua área corporal não coberta (considerando que ele esteja vestindo uma sunga).
Ao contrário do aviso comum de que o filtro solar deve ser reaplica a cada 2-3 horas, uma pesquisa mostrou que a melhor proteção é alcançada com a aplicação 15-30 antes da exposição, seguida por uma reaplicação 15-30 minutos depois que a exposição ao sol começar. Mais reaplicações só são necessárias depois de atividades como natação, ou que a pessoa sue.
Entretanto, estudos mais recentes da Universidade da Califórnia indicam que o filtro solar deve ser reaplicado em duas horas para que mantenha sua efetividade. A não-reaplicação poderia causar até mais dano às células do que o não uso do filtro solar, devido à liberação de radicais livres extras emitidos por substâncias químicas presentes no filtro.
Uma redução significante à exposição solar inibe a produção de Vitamina D. Entretanto, a exposição ao sol excessiva tem sido conclusivamente relacionada a algumas formas de câncer de pele e sinais de envelhecimento precoce. A estação, latitude, hora do dia, cobertura de nuvens, tipo de pele e filtro solar, todos têm efeito na produção da vitamina D na pele, mas quinze minutos por dia de exposição direta ao sol geralmente é aceito entre os médicos para se atingir um ótimo na produção de vitamina D. Os especialistasgeralmente recomendam uma caminhada de 15 minutos pela manhã ou final de tarde sem a utilização de filtro solar, para atingir essa necessidade.
Mecanismo de ação
Os principais ingredientes dos filtro solares são moléculas aromáticas conjugadas com grupos carbonil. Essa estrutura geral permite à molécula absorver raios ultravioleta de alta energia e liberar a energia como raios de baixa energia, desse modo prevenindo o ultravioleta, que é danoso à pele, de atingi-la. Então, quando da exposição à luz UV, a maioria dos ingredientes (com a exceção do avobenzona) não sofrem uma modificação química significativa, permitindo estes ingredientes reter o potencial de absorção de UV sem uma fotodegradação significante.
Tem dois tipos de “protetor” solar: o “químico” e o “físico”. O físico, muitas vezes chamado de bloqueador solar, contém maior quantidade de dióxido de titânio, que cria uma barreira para a passagem dos raios UV, ou seja funciona como um refletor – esses bloqueadores são aqueles que deixam uma camada branca sobre a pele, devido ao excesso de TiO2. Já os protetores químicos possuem substâncias que interagem com a radiação UV absorvendo-a e sofrendo mudanças em suas estruturas; assim a radiação UV é absorvida por essa fina camada de substâncias e não atinge os melanócitos – esse protetores não deixam aquela camada tão branca quanto os bloqueadores.
Fator de Proteção Solar
O FPS (Fator de Proteção Solar) é uma medida de laboratório que indica a efetividade do filtro solar; quanto mais alto o valor do FPS; maior a proteção que o filtro solar oferece contra raios UV-B (a radiação ultravioleta que causa a queimadura solar) e UVA (mais associada aos danos de longo prazo na pele). O FPS indica a relação entre o tempo que a pessoa pode se expor à luz solar usando filtro solar antes de se queimar e o tempo que ela pode ficar exposta à luz solar sem se queimar. Por exemplo, uma pessoa que se queimaria depois de 12 minutos no sol deve se queimar 2 horas (120 minutos) se protegida com um filtro solar de FPS 10 (10 vezes mais proteção). Na prática, a proteção de um filtro solar depende de fatores como:
- O tipo de pele (cor) do usuário.
- A quantidade que é aplicada e a freqüência de reaplicação.
- Atividades que o usuário faz (por exemplo, nadar leva a uma perda de filtro solar da pele).
- Quantidade de filtro solar que a pele absorve.
Para escolher o FPS deve se relevar as seguintes condições as pessoas têm que usar, no mínimo, FPS 15, inclusive quem tem pele mais morena defesa feita por unaniminidade pelos dermatologistas. A regra é: quanto mais clara for a pele, mais alto deve ser o FPS. Os dermatologistas garantem que vale a pena investir nos fatores de proteção mais altos, mesmo que as diferenças de proteção não sejam muito grandes -o FPS 15 filtra 93,3% da radiação ultravioleta B, enquanto o FPS 30 evita 96,7%. “Ainda não é possível se proteger 100%, porém com valores mais altos se consegue um aumento do espectro de proteção”, diz o dermatologista Humberto Ponzio.
O FPS é uma medida imperfeita do dano à pele porque um dano invisível e envelhecimento da pele também é causado pelo muito comum ultravioleta tipo A, que não causa vermelhidão nem dor. Os filtro solares convencionais não bloqueiam o UVA tão efetivamente quanto o UVB, e mesmo taxas de FPS acima de 30 podem significar baixos níveis de proteção contra UVA, de acordo com um estudo realizado em 2003 feito por pesquisadores. De acordo com outro estudo de 2004, o UVA também causa danos ao DNAde células mais profundas da pele, aumentando o risco de ocorrer melanoma maligno. Até mesmo alguns produtos rotulados como “proteção contra o amplo espectro UVA/UVB”, não provêm boa proteção contra raios UVA . A melhor proteção contra o UVA é provida por produtos que contêm óxido de zinco, avobenzona e mexoryl®. Dióxido de titânio provavelmente provê boa proteção, mas não cobre todo espectro do UVA.
Devido à confusão criada pelos consumidores sobre o grau verdadeiro e a duração da proteção oferecida, restrições nos rótulos do produtos são impostas em vários países. NosEstados Unidos em 1999, a Food and Drug Administration (FDA) decidiu instituir o rótulo de FPS 30+ para filtros que oferecem mais proteção, e uma restrição similar foi tomada na Austrália. Essa atitude foi tomada para desencorajar empresas a produzirem falsos títulos com relação ao nível de proteção oferecida (tal como “proteção o dia inteiro”), e porque um filtro com FPS acima de 30 não provê proteção significamente maior [3].
O FPS pode ser medido aplicando-se o filtro na pele de um voluntário e medindo-se quanto tempo leva até que ocorra queimadura ao ser exposto a uma luz solar artificial. Nos EUA, tal teste in vitro é requisitado pela FDA. Também pode-se medir in vitro com a ajuda de um espectroscópio especialmente desenvolvido. Neste caso, a verdadeira transmitância do filtro é medida, juntamente com a degradação do produto devido à exposição à luz solar. Nessa medição, a transmitância do filtro deve ser medido sob todos comprimentos de onda na faixa do UVB (290–350 nm), juntamente com a tabela de quão efetivos os vários comprimentos de onda causam queimaduras (o espectro de ação eritemal) e a verdadeira intensidade espectro da luz solar (veja a figura). Tais medições in vitro apresentam muito boa concordância com as medições in vivo. [4]
Matematicamente, o FPS é calculado de dados medidos como: 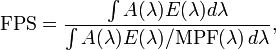 onde E(λ) é o espectro de radiação solar, A(λ) é o espectro de ação eritemal, e MPF(λ) é o fator de proteção monocromática, todas funções do comprimento de onda λ. O MPF é grosseiramente o inverso da trasmitância num dado comprimento de onda.
onde E(λ) é o espectro de radiação solar, A(λ) é o espectro de ação eritemal, e MPF(λ) é o fator de proteção monocromática, todas funções do comprimento de onda λ. O MPF é grosseiramente o inverso da trasmitância num dado comprimento de onda.
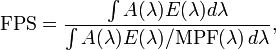 onde E(λ) é o espectro de radiação solar, A(λ) é o espectro de ação eritemal, e MPF(λ) é o fator de proteção monocromática, todas funções do comprimento de onda λ. O MPF é grosseiramente o inverso da trasmitância num dado comprimento de onda.
onde E(λ) é o espectro de radiação solar, A(λ) é o espectro de ação eritemal, e MPF(λ) é o fator de proteção monocromática, todas funções do comprimento de onda λ. O MPF é grosseiramente o inverso da trasmitância num dado comprimento de onda.
A fórmula acima demonstra que o FPS não é simplesmente o inverso da transmitância na região do UVB. Se isso fosse verdade, aplicar duas camadas de FPS 5 deveria ser equivalente ao FPS 25 (5×5). A verdadeira combinação de FPS é sempre menor que o quadrado de uma camada única de FPS.
Fonte: Wikipédia.org apud http://www.vocesabia.net/curiosidades/como-funciona-o-filtro-solar/
Como fazer gelo rapidamente? – Efeito Mpemba!
Colocam-se dois recipientes iguais (de preferência transparentes) com a mesma quantidade de água no congelador. Um com água fria outro com água quente (40 ou 50ºC). O recipiente que contém água quente congela primeiro!
O Efeito Mpemba!
Numa escola na Tanzânia em 1969, um aluno de nome Erasto Mpemba e um colega, devido a um trabalho escolar, estavam a fazer gelado. Como estavam com pressa Mpemba colocou a sua mistura no congelador sem a deixar arrefecer e o seu colega nem sequer a chegou a aquecer a dele. Ao contrário do que seria de esperar o gelado de Mpemba solidificou em primeiro lugar.
Explicação do Fenómeno:
Quando confrontados com esta questão pela primeira vez somos impelidos a achar que se trata de um disparate. Se a temperatura da água num recipiente A é superior à temperatura da água noutro recipiente B então a água em A vai atingir o ponto de congelação mais tarde que a água em B, demorando mais tempo a ficar sólida… Quando confrontada com a realidade esta explicação mostra-se, como se pode observar experimentalmente, demasiado simples. Verifica-se, pois, que o abaixamento da temperatura de um líquido não é um processo assim tão linear pelo que há que ter em conta outros factores que, apesar de tudo, não deixam de ter um quê de especulativos:
Convecção e superfície isolante
Evaporação
Má Condução
Gases dissolvidos
Boa condução e bom contacto
Existe a teoria de que uma camada fina de gelo na superfície de um recipiente pode atrasar o processo de arrefecimento.
Convecção e superfície isolante
Evaporação
Pensa-se que a evaporação é um factor que permite que a água morna congele mais rapidamente do que a água fria. A água morna ou quente evapora mais facilmente do que a água fria. Assim a evaporação não só reduz, ligeiramente, a quantidade de água quente a congelar como provoca um abaixamento na temperatura da mesma devido à perda de calor.
Má Condução
Se o recipiente for de um material que seja um mau condutor térmico, como a madeira, a refrigeração da água será na sua maior parte devida evaporação em vez da condução. Este poderia ser um factor importante na explicação de como a água quente congela mais rapidamente do que a água fria. Vimos que a água quente tem vantagem neste particular… Mpemba usou covetes de madeira quando fazia o seu gelado e observou o fenómeno.
Gases dissolvidos
Um outro factor tem a ver com o facto de a água possuir gases dissolvidos, tais como o oxigénio e o dióxido de carbono, cujo o efeito é baixar o seu ponto de congelação. Quando a água é aquecida, os gases são expelidos uma vez que a sua solubilidade em água diminui a altas temperaturas. Assim, quando a água quente arrefece, tem menos gás dissolvido do que a água que não foi aquecida, assim há um aumento do seu ponto de congelação. pelo que congela primeiro!
Experimente!:
Para se testar este efeito é necessário manter todos os factores constantes (excepto a temperatura da água). Neste caso para duplicarmos o Efeito Mpemba em casa devemos manter constantes os seguintes parâmetros:
A temperatura do congelador
A quantidade de água colocada no recipiente
O tamanho, forma e material do recipiente
Qualquer tipo de movimento do ar sobre a água.
O tamanho, forma e material do recipiente
Qualquer tipo de movimento do ar sobre a água.
| QUAL O ELEMENTO QUÍMICO MAIS ABUNDANTE NA TERRA? | |
O elemento químico mais abundante na Terra é o oxigênio, que compõe cerca de 49,5% da massa da crosta terrestre, da água e da atmosfera terrestre.
O elemento que fica em segundo lugar é o silício. O dióxido de silício e os silicatos fazem parte de cerca de 87% dos compostos que existem na crosta terrestre. | |
35ª REUNIÃO ANUAL DA SOCIEDADE BRASILEIRA DE QUÍMICA
Águas de Lindóia – SP, 28 a 31 de maio de 2012
A 35ª Reunião Anual da Sociedade Brasileira de Química (35ª RASBQ) será realizada em Águas de Lindóia – SP, de 28 a 31 de maio de 2012. O tema central será "Responsabilidade, Ética e Progresso Social". Seguindo uma tradição de mais de três décadas, as RASBQs contam com grande participação da comunidade química brasileira e de áreas afins, o que tem garantido seu contínuo sucesso.
A programação da 35ª RASBQ contará com uma conferência de abertura, 13 conferências convidadas, 1 simpósio, 4 sessões temáticas, 11 minicursos, 16 sessões coordenadas, 3 sessões de painéis, 12 workshops, assembleias regionais e divisionais, assembleia geral, além de sessões especiais, premiações e lançamentos de livros. Assim, com uma atmosfera calorosa e acolhedora, pretendemos promover a máxima integração entre estudantes de graduação e pós-graduação, pesquisadores e professores. São esperados mais de três mil participantes para apresentação e discussão de trabalhos inéditos de pesquisa.
Um grande objetivo da Comissão Organizadora foi adotar medidas práticas capazes de atender às reivindicações da Assembleia Geral Ordinária da 34ª RASBQ para melhoria da infraestrutura e da qualidade da sessão de painéis que, sem dúvida, é uma das mais importantes atividades de nossas Reuniões Anuais. Desta forma, na 35ª RASBQ o espaço será aperfeiçoado e o tempo para apresentação dos painéis será aumentado. Além disso, foi aprovado pela Diretoria e Conselho da SBQ que cada inscrição dará direito a submissão de 1 trabalho. Assim, afirmamos o nosso compromisso com a criação de um ambiente favorável para a consolidação de debates e discussões científicas de alto nível.
Em 2012 a SBQ estará comemorando seus 35 anos de fundação, um motivo a mais para celebrarmos o grande momento da química brasileira com uma festa especial na abertura da 35ª RASBQ. Aguardem.
Esperamos contar com a valiosa participação e o apoio de todos!
Até maio de 2012!
Adriano D. Andricopulo
Secretário Geral da SBQ
Presidente da Comissão Organizadora da 35ª RASBQ
A programação da 35ª RASBQ contará com uma conferência de abertura, 13 conferências convidadas, 1 simpósio, 4 sessões temáticas, 11 minicursos, 16 sessões coordenadas, 3 sessões de painéis, 12 workshops, assembleias regionais e divisionais, assembleia geral, além de sessões especiais, premiações e lançamentos de livros. Assim, com uma atmosfera calorosa e acolhedora, pretendemos promover a máxima integração entre estudantes de graduação e pós-graduação, pesquisadores e professores. São esperados mais de três mil participantes para apresentação e discussão de trabalhos inéditos de pesquisa.
Um grande objetivo da Comissão Organizadora foi adotar medidas práticas capazes de atender às reivindicações da Assembleia Geral Ordinária da 34ª RASBQ para melhoria da infraestrutura e da qualidade da sessão de painéis que, sem dúvida, é uma das mais importantes atividades de nossas Reuniões Anuais. Desta forma, na 35ª RASBQ o espaço será aperfeiçoado e o tempo para apresentação dos painéis será aumentado. Além disso, foi aprovado pela Diretoria e Conselho da SBQ que cada inscrição dará direito a submissão de 1 trabalho. Assim, afirmamos o nosso compromisso com a criação de um ambiente favorável para a consolidação de debates e discussões científicas de alto nível.
Em 2012 a SBQ estará comemorando seus 35 anos de fundação, um motivo a mais para celebrarmos o grande momento da química brasileira com uma festa especial na abertura da 35ª RASBQ. Aguardem.
Esperamos contar com a valiosa participação e o apoio de todos!
Até maio de 2012!
Adriano D. Andricopulo
Secretário Geral da SBQ
Presidente da Comissão Organizadora da 35ª RASBQ
terça-feira, 24 de abril de 2012
Antidetonantes
Os antidetonantes são substâncias químicas que são adicionadas à gasolina com a finalidade de aumentar o seu índice de octanagem, isto é, a sua resistência.
Conforme dito no texto “Número de Octanagem de Combustíveis”, a octanagem de uma gasolina mede a sua qualidade, baseado na sua resistência à compressão dentro do motor de explosão interna.
Além disso, o índice de octanagem é uma escala na qual se compara a resistência da gasolina com a resistência do heptano (zero) e do isoctano (100). Assim, se tivermos um índice de octanagem igual a 70, significa que a resistência à compressão da gasolina é a mesma de uma mistura de 70% de isoctano e 30% de heptano.
Entretanto, existem algumas gasolinas especiais que apresentam um índice de octanagem superior a 100. Isso é possível graças à adição de antidetonantes a essas gasolinas.

O próprio nome já diz, eles impedem a detonação ou combustão da gasolina antes da hora certa, que é quando a vela do motor de combustão interna de quatro tempos solta a faísca. Antes disso, ela está sendo comprimida e o antidetonante “ajuda” a gasolina a não explodir durante essa compressão; o que acarretaria em menor potência para o motor.
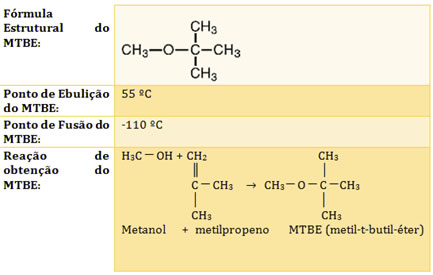
O Conselho Nacional do Petróleo (CNP) autorizou a Petrobrás a aditivar a gasolina usando o composto metil-t-butil-éter (MTBE) até 7% em volume para aumentar o índice de octanagem.
Veja algumas informações relacionadas a esse antidetonante na tabela a seguir:
Por Jennifer Fogaça
Graduada em Química
Assinar:
Postagens (Atom)
.JPG)





